2019年5月27号,微生物合成与定量生物学实验室在国际生物化学与分子生物学著名杂志Nucleic Acids Research发表了题为“Maintenance of translational elongation rate underlies the survival of Escherichia coli during oxidative stress”的研究长文。戴雄风博士为论文的通讯作者,朱曼璐博士为论文的第一兼共同通讯作者。我院为唯一作者单位。

在自然界中,细菌需要对抗各种逆境环境,包括高温、氧化、强酸以及高渗透压。研究细菌如何应对外在的逆境是微生物学研究的热点。从分子水平来说,逆境响应的研究主要关注鉴定响应逆境的各种基因。分子微生物学家将主要的精力花在研究具体的逆境信号响应途径。然而一些根本的围绕细菌逆境生理的问题尚无较好的回答:逆境抑制生长的本质原因是什么?细菌的逆境响应如何缓解这个问题?决定细菌在逆境中存活极限的内在限制因素是什么?
在该项研究中,研究者主要关注一种常见的逆境——氧化胁迫对大肠杆菌的抑制作用。ROS(活性氧)一直拥有广泛的关注度,它对于所有类型的细胞包括细菌、酵母、植物细胞以及动物细胞都可以造成严重的损伤。对于我们人类来说,活性氧一直被认为与多种影响生命健康的重大疾病如心脑血管疾病、神经退行性疾病、癌症、炎症、关节炎等息息相关。其中,活性氧被认为是介导生物衰老的罪魁祸首之一。当各种类型的细胞(从原核生物到真核生物细胞)遭遇氧化胁迫时,一个最明显的表征即为生长抑制。之后,细胞需要建立逆境响应防御体系来清除自由氧,进而恢复生长。然而,当氧化胁迫程度较高时,细胞将无法存活。这里有一个本质的生理学问题尚无较好的回答——决定细胞耐受氧化胁迫极限的生理学关键因素是什么?
以大肠杆菌为研究对象,采用定量生物学手段,该研究对这个重要问题进行了深入的剖析。研究首先采用了不同浓度的过氧化氢处理指数生长中的细菌,发现在低浓度到中等浓度(0-5 mM)的过氧化氢条件下,细菌生长首先完全停滞,然而经过一段迟滞期(lag time)后即可以完全恢复生长(lag time随着过氧化氢浓度增加而显著延长)。然而当过氧化氢浓度达到一个阈值(6 mM)时,此时细菌生长彻底停滞并失去了恢复生长的能力。深入的研究表明,过氧化氢胁迫造成了细菌tRNA的急剧降解,进一步导致了核糖体翻译延伸速率的极大降低(正常条件为17 aa/s,在5 mM条件下可以降低到1 aa/s以下),全局性地抑制了细菌的逆境防御体系。核糖体翻译延伸速率的降低导致细菌合成oxyR regulon相关逆境响应蛋白的显著滞后。而在阈值浓度下(6 mM),核糖体的翻译延伸彻底停滞,导致细菌氧化胁迫防御体系的全局性崩溃,进而无法在氧化胁迫中存活。
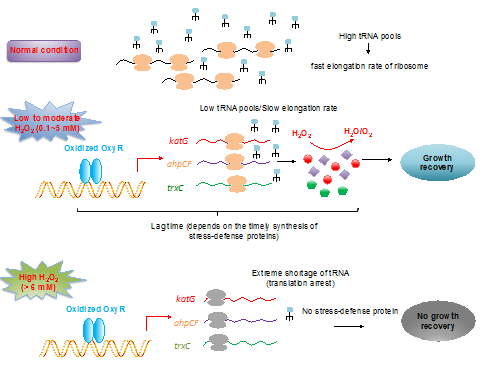
图1: 过氧化氢介导的氧化胁迫抑制细菌的逆境响应过程进而抑制细菌的存活
该研究的重要贡献在于首次揭示了核糖体翻译延伸过程是决定细菌能否经受氧化胁迫的关键性生理指标。以往对逆境生理的研究主要集中在转录水平的响应(比如全局逆境响应体系,RpoS regulon),而该项研究是目前为此首次发现一种特定的逆境可以在翻译水平抑制细菌的逆境响应过程,证明了细菌维持核糖体“速度”的重要生理性意义。
该研究是微生物定量与合成生物学实验室今年第二次在Nucleic Acids Research发文,此前3月27号,课题组发表了题为题为“Growth suppression by altered (p)ppGpp levels results from non-optimal resource allocation in Escherichia coli”的研究论文,揭示了“魔斑”(p)ppGpp对细菌生长、蛋白质翻译与基因表达的全局调控作用。该项研究也延续了该课题组过去在核糖体翻译效率控制领域的系列重要进展。在以往的研究中,他们对大肠杆菌进行了有史以来最为系统的翻译延伸效率的定量研究,系统界定了决定翻译效率的三个关键指标即翻译延伸速率、核糖体含量以及活性核糖体比例三者与生长速率的关系及控制模式(Dai et al 2017 Nature Microbiology);建立了一种简单方便的核糖体翻译延伸速率的定量方法(Zhu et al 2016 Nucleic Acids Research)并揭示了高渗胁迫对细菌蛋白质翻译效率的抑制模式(Dai et al 2018 mBio);在这些工作的基础上进一步形成了细菌生长与核糖体合成、蛋白质翻译效率内在联系的理论预测模型(Zhu & Dai 2018 Critical Rev Microbiol)。
相关文章链接:
https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkz467/5498755
https://academic.oup.com/nar/article/47/9/4684/5420536?searchresult=1
https://www.nature.com/articles/nmicrobiol2016231
https://academic.oup.com/nar/article/44/20/e155/2607980?searchresult=1
https://mbio.asm.org/content/9/1/e02375-17
https://www.tandfonline.com/doi/abs/10.1080/1040841X.2018.1425672?journalCode=imby20